Уполномоченный представитель
До введения медицинских изделий в обращение на рынок Украины, производитель-нерезидент должен назначить Уполномоченного представителя, которым может быть юридическое лицо либо физическое лицо-предприниматель резидент Украины.
Уполномоченный представитель в Украине является связующим звеном между Украиной (органами по оценке соответствия, органом рыночного надзора, органами доходов и сборов, потребителями и пр.) и производителем, обеспечивает своевременный обмен информацией, выполняет постмаркетинговый надзор.
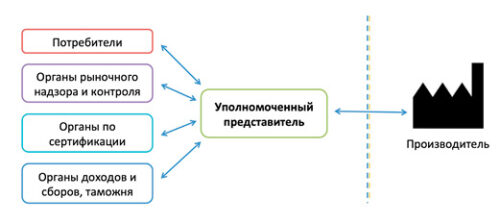
Уполномоченный представитель
Уполномоченный представитель — любое юридическое лицо или физическое лицо-предприниматель, являющееся резидентом Украины или зарегистрированное в соответствии с законодательством Украины, представительство иностранного субъекта, имеющее надлежащим образом подтвержденные полномочия производителя совершать юридические действия от его имени относительно обязанностей производителя, установленных Техническим регламентом.
У уполномоченного представителя есть множество прав и обязательств: хранить техническую документацию не менее 5 лет (15 лет для активных имплантируемых изделий) с моменты выпуска последнего изделия, участвовать в проверках органов рыночного надзора и оплачивать штрафы за производителя, выполнять пост-маркетинг и уведомлять об инцидентах, авторизировать импортеров, блокировать серый импорт и пр.
Обязательства и ответственность описаны в Технических регламентах на медицинские изделия, Законе “Про государственный рыночный надзор и контроль непищевой продукции” и других законодательных актах. Приказом МОЗ Украины №142 от 22.01.2020 утверждены Методические рекомендации “Уполномоченный представитель”, разработанные на основании Руководящего документа Европейской Комиссии MEDDEV 2.5/10 от января 2012 года, но не являющиеся юридически обязательными.
Назначение Уполномоченного представителя не изменяет ответственности производителя. Уполномоченный представитель должен быть назначен и находиться под наблюдением производителя.
Каждое медицинское изделие (тип/модель) должно быть связано только с одним Уполномоченным представителем. Производитель может назначить нескольких Уполномоченных представителей, но для разных медицинских изделий.
Название и местонахождение уполномоченного представителя должно быть размещено на упаковке каждого медицинского изделия и/или в инструкции по применению. Для улучшения связи с потребителем мы также рекомендуем указывать номер телефона, е-мейл и вебсайт. Также название и адрес уполномоченного представителя будут указаны в декларации и сертификате соответствия.
Уполномоченным представителем может выступить импортер или дистрибьютор, либо третья организация. Некоторые производители имеют внутренее правило, согласно которому уполномоченным представителем не может быть организация, участвующая в цепи поставки продукции. Также, если производитель работает с несколькими дистрибьюторами, назначение одного из них уполномоченным представителем дает существенное конкурентное преимущество, так как его название и адрес будут на маркировке всех поставляемых в Украину изделий.
Договор и Доверенность
Назначение уполномоченного представителя выполняется в письменном виде Доверенностью и/или Договором. Доверенность должна быть надлежащим образом заверена и легализована.
Мы рекомендуем использовать оба документа:
- Доверенность имеет меньший объем, ее удобно использовать для подачи во внешние организации, однако Доверенность передает права только в одностороннем порядке.
- Договор может регулировать права и обязанности обеих сторон, ограничить ответственность уполномоченного представителя в отношении качества и безопасности медицинских изделий, установить сроки коммуникации, порядок взаимодействия с рекламациями и сообщениями о нежелательных явлениях, многих других аспектах.
Договор назначения уполномоченного представителя не равнозначен договору на импорт/дистрибуцию и обычно является отдельным документом, по своей структуре более напоминающим операционную процедуру. В некоторых случаях Договор назначения уполномоченного представителя может быть приложением к Договору на импорт и дистрибуцию.
Наш юрист подготовит проект Доверенности и/или Договора на назначение Уполномоченного представителя в Украине, ответит на вопросы производителя, пояснит требования к легализации и сопроводит подписание. Мы постоянно следим за обновлениями и вовремя реагируем на основные замечания со стороны таможни, органов рыночного надзора и органов по оценке соответствия.
Регистрация уполномоченного представителя
В некоторых случаях данные о лице, ответственном за введение в обращение медицинских изделий, подлежат регистрации в компетентном органе — Государственной Службе Украины лекарственных средств и контролю за наркотиками (ГосЛекСлужба).
Регистрация проводится до введения в обращение:
- медицинских изделий I-го класса, в том числе стерильных и/или с функцией измерения;
- процедурных наборов;
- всех медицинских изделий для диагностики in-vitro.
Порядок регистрации описан в Технических регламентах и Приказе МОЗ Украины №122 от 10.02.2017 года. Реестр публикуется в электронном виде на веб-сайте ГосЛекСлужбы.
Производитель или Уполномоченный представитель должны проинформировать Гослекслужбу о намерениях провести клинические исследования. Они также информируют об окончании таких исследований и предоставляют письменный отчет.
Обязанности и ответственность
Обязанности Уполномоченного представителя описаны как в Технических регламентах на медицинские изделия, так и в смежных законодательных актах. Список основных обязанностей:
- Нести ответственность за медицинские изделия, введенные в обращение.
- Взаимодействовать с органами рыночного надзора, правоохранительными и другими компетентными органами от имени производителя.
- Хранить документацию не менее 5 лет (15 лет для активных имплантируемых изделий) с момента выпуска последнего изделия на рынок и предоставлять в компетентные органы.
- Выполнять пост-маркетинг:
- собирать данные об инцидентах на рынке Украины и уведомлять производителя,
- подавать в компетентный орган данные обо всех серьезных инцидентах в Украине и мире, которые могли или привели к смерти пользователя или существенному ухудшению здоровья,
- технические или медицинские причины, которые приводят к систематическим отзывам продукции.
- Выполнять корректирующие и ограничивающие действия в отношении продукции.
- Информировать компетентный орган о корректирующих действиях и отзыве продукции.
- Оплачивать штрафы за введение в обращение несоответствующей продукции.
Уполномоченный представитель является представителем производителя и несет ответственность согласно украинского законодательства и Договора с производителем.
Штрафы установлены статьей 44 Закона Украины “Про государственный рыночный надзор и контроль непищевой продукции”:
- Введение в обращение продукции, представляющей серьезный риск — 102 000 грн.
- Введение в обращение продукции, не соответствующей установленным требованиям — 51 000 грн.
- Невыполнение или неполное выполнение решения о принятии ограничительных (корректирующих) мер в отношении продукции, представляющей серьезный риск — 170 000 грн.
- Невыполнение или неполное выполнение решения о принятии ограничительных (корректирующих) мер в отношении прочей продукции — 102 000 грн.
- Создание препятствий путем недопущения к проведению проверок характеристик продукции — 170 000 грн.
Штрафы накладываются за каждую модель, артикул или партию продукции, которая является опасной, представляет риск и/или не соответствует установленным требованиям, независимо от количества единиц такой продукции и/или мест реализации.
Аутсорсинг услуги Уполномоченного представителя
Если производитель по каким-либо причинам не может назначить дистрибутора уполномоченным представителем, либо сотрудничает с несколькими дистрибьюторами — мы можем взять на себя данную роль. Компания “Кратия Медтехника” специализируется на выполнении функций Уполномоченного представителя, сертифицирована по стандарту ISO 9001:2017, имеет штат компетентных специалистов.
Мы не вовлечены в товаропроводящие процессы, что гарантирует отсутствие конфликта интересов и профессиональное выполнение обязательств. Наша ответственность перед третьими лицами застрахована согласно Договора добровольного страхования профессиональной ответственности.
Выделенный веб-сайт: https://uarep.com/
Для начала сотрудничества или получения консультации Вы можете связаться с нами:
- по телефонам +38 044 361-48-28, +38 044 221-71-29,
- по e-mail info@cratia.ua,
- или приехать на встречу к нам в офис.

